-
الدرس 2 بنــيــة الــــذرة - الكهرباء
☻لمحة تاريخية
مند حوالي القرن الرابع قبل الميلاد طرحت أول نظرية حول الذرة والتي تقول
المواد تتكون من جسيمات متناهية في الصغر لا ترى ولا تقبل التقسيم
أطلق عليها إسم الذرة
ATOMOS☻ مكونات الذرة
في بداية القرن العشرين بدأت الإكتشافات الكبرى حول الذرة
طومسون إكتشف أن الذرة تحتوي على دقائق صغيرة جدا سماها الإلكترونات وهي تحمل كهرباء سالبة
روثرفورد إكتشف أن الذرة تتكون من نواة تحمل كهرباء موجبة كتلتها تساوي كتلة الذرة وقطرعا صغير جدا بالمقارنة مع قطر الذرةإستنتاج
تتكون الذرة من نواة وإلكترونات يفصل بينهما فراغ
النواة تتوسط الذرة تحتوي على شحنات موجبة قطرها صغير جدا مقارنة مع قطر الذرة
الإلكترونات وهي دقائق صغير جدا مشحونة بكهرباء سالبة تدور حول النواة سرعة الضوء تقريبا يرمز للإلكترون ب -e ولشحنته ; e-
 نماذج الذرة
نماذج الذرة النمودج الحالي و نمودج بوهر
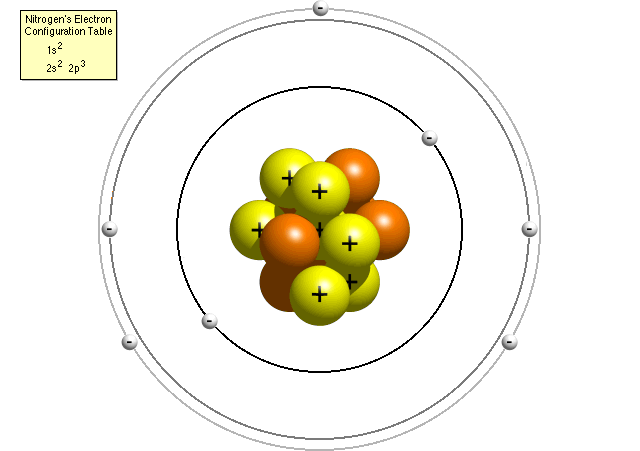
ملحوظة النموذج الحالي يعتبر أن الإلكترونات ليس لها مسارا ثابتا وبذلك أطلق على مساراتها بالسحابة الإلكترونية
 التعادل الكهربائي في الذرة
التعادل الكهربائي في الذرةشحنة الذرة شحنة الإلكترونات شحنة النواة العدد الذري z الرمز إسم الذرة 0e -1e +1e z=1 H الهيدروجين 0e -8e +8e z=8 O اوكسجين 0e -26e +26e z=26 Fe حديد 0e -13e +13e z=13 Al الالومنيوم الذرات تختلف فيما بينها باختلاف نواها وعدد إلكتروناتها
جميع الذرات متعادلة كهر بائيا بمعنى ان عددالشحنات الموجبة المتواجدة في النواة يساوي عدد الإلكترونات التي تدور حول نواتها
ويسمى العدد الذري z يرمز لعدد الشحنات الموجبة في النواة بالحرف☻الأيونات
الأيونات نوعان ذرات فقدت إلكترون أو اكثر وذرات إكتسبت إلكترون او أكثر
الكاتيونات ♣
يرمز لها برمز الذرة التي فقدت الإلكترونات مع إضافة إشارات + تدل على عدد الإلكترونات المفقودة يمين أعلى الرمز
♣الأنيونات
يرمز لها برمز الذرة التي اكتسبت الإلكترونات مع إضافة عدد من إشارات -يمين أعلى الرمز تدل على عدد الإلكترونات المكتسبة
جدول توضيحي شحنته الكهربائية العدد الذري نوعه صيغته إسم الأيون +2e Z=29 كاتيون Cu2+ ايون النحاس اا +3e Z=26 كاتيون Fe3+ ايون الحديد ااا -1e Z=17 أنيون Cl- أيون الكلورور +3e Z=13 كاتيون Al3+ أيون الألومنيوم ااا -2e Z=8 أنيون O2- ايون الاوكسجين
الأيونات المتعددة الذرات
♣جدول توضيحي 
شحنة الأيون نوع الأيون رمز الأيون إسم الأيون -1e OH- أيون الهيدروكسيد -2e SO42- أيون الكبريتات -1e NO3- أيون النترات +1e NH4+ أيون الأمونيوم استنتاج
الأيونات المتعددة الذرات هي مجموعة من الذرات اكتسبت أو فقدت إلكترون أو أكثر
-
Commentaires
2hassena wissameLundi 12 Octobre 2015 à 22:38fuyuigfyuشكرا جزيلا استاذي الفاضل بفضلك نحن متميزين في هذه المادة لك كل التقدير والاحترام
-
yosraMercredi 24 Février 2021 à 20:25thank you
-
4iman jaoumaMardi 10 Novembre 2015 à 01:25merci beaucoup
-
Mercredi 11 Novembre 2015 à 00:47
pas de quoi j aimerais bien me poser des questions pertineuses et me signaler s il ya une faute
-
5aymane mokfiVendredi 8 Juillet 2016 à 00:34merci6saadDimanche 2 Octobre 2016 à 12:077reda byadMardi 18 Octobre 2016 à 23:018Mariam OmriMardi 1er Novembre 2016 à 22:24C sympa merci10emnaMardi 2 Janvier 2018 à 19:3711yosraMercredi 24 Février 2021 à 20:25merci Suivre le flux RSS des commentaires
Suivre le flux RSS des commentaires
 Ajouter un commentaire
Ajouter un commentaire
بسم الله الرحمان الرحيم


thanks
