-
Par sc.physiques le 7 Septembre 2013 à 23:44
التمييز بين الجسم والمادة
أمثلة
باب من حديد وخشب
مزهرية من فخار
مزهرية من نحاس
نافذة من البلاستيك والألومنيومإستنتاج جميع الأجسام تتكون من مواد
المواد الأكثر إستعمالا لصناعة الأجسام هي الفخار الخشب الزجاج البلاستيك والفلزاتالخواص الفيزيائية لبعض المواد
خواص الفلزات
خواصها المشتركة
الفلزات مثل الحديد النحاس الالومنيوم الدهب القصدير لها خصائص مشتركة ندكرها ما يلي
البريق الفلزي
التوصيل الحراري والكهربائيالخواص المميزة لبعض الفلزات
خواص أخرى قابلية التمغنط الكتلة الحجمية نقطة الإنصهار المظهر الفلز لايقبل الطرق إلإ بعد التسخين يتمغنط 7.8g/cm3 1536°C رمادي الحديد يقبل الطرق دون تسخينه لا 8.9g/cm3 1083°C أحمر أجوري النحاس يمكن أن تصنع منه ورقة رقيقة لا 2.7g/cm3 658°C أبيض فضي الألومنيوم الزجاج والبلاستيك
خاصيات الزجاج
مادة تصنع من الرمل وبذلك يعتبر الزجاج صديق للبيئة لكنه ليس كذلك لانه يسهلك كميات كبيرة من الطــــاقة يعني كميات كبير ة من غاز ثنـائي اوكسيد الكربون ينفث في الجو .سهـــــــل التدوير حتـــى في الدول النامية
خاصيات البلاستيك
يتم تصنيع البلاستيك من البترول الخام وبذلك يعتبرونه من أشد الأعداء للبيئة وفيه أنواع مختلفة نذكر منها
PVC PS PE
lien
 votre commentaire
votre commentaire
-
Par sc.physiques le 12 Septembre 2013 à 00:45
☻لمحة تاريخية
مند حوالي القرن الرابع قبل الميلاد طرحت أول نظرية حول الذرة والتي تقول
المواد تتكون من جسيمات متناهية في الصغر لا ترى ولا تقبل التقسيم
أطلق عليها إسم الذرة
ATOMOS☻ مكونات الذرة
في بداية القرن العشرين بدأت الإكتشافات الكبرى حول الذرة
طومسون إكتشف أن الذرة تحتوي على دقائق صغيرة جدا سماها الإلكترونات وهي تحمل كهرباء سالبة
روثرفورد إكتشف أن الذرة تتكون من نواة تحمل كهرباء موجبة كتلتها تساوي كتلة الذرة وقطرعا صغير جدا بالمقارنة مع قطر الذرةإستنتاج
تتكون الذرة من نواة وإلكترونات يفصل بينهما فراغ
النواة تتوسط الذرة تحتوي على شحنات موجبة قطرها صغير جدا مقارنة مع قطر الذرة
الإلكترونات وهي دقائق صغير جدا مشحونة بكهرباء سالبة تدور حول النواة سرعة الضوء تقريبا يرمز للإلكترون ب -e ولشحنته ; e-
 نماذج الذرة
نماذج الذرة النمودج الحالي و نمودج بوهر
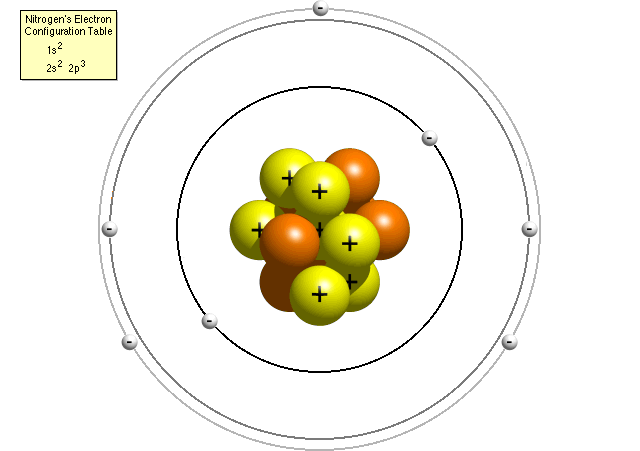
ملحوظة النموذج الحالي يعتبر أن الإلكترونات ليس لها مسارا ثابتا وبذلك أطلق على مساراتها بالسحابة الإلكترونية
 التعادل الكهربائي في الذرة
التعادل الكهربائي في الذرةشحنة الذرة شحنة الإلكترونات شحنة النواة العدد الذري z الرمز إسم الذرة 0e -1e +1e z=1 H الهيدروجين 0e -8e +8e z=8 O اوكسجين 0e -26e +26e z=26 Fe حديد 0e -13e +13e z=13 Al الالومنيوم الذرات تختلف فيما بينها باختلاف نواها وعدد إلكتروناتها
جميع الذرات متعادلة كهر بائيا بمعنى ان عددالشحنات الموجبة المتواجدة في النواة يساوي عدد الإلكترونات التي تدور حول نواتها
ويسمى العدد الذري z يرمز لعدد الشحنات الموجبة في النواة بالحرف☻الأيونات
الأيونات نوعان ذرات فقدت إلكترون أو اكثر وذرات إكتسبت إلكترون او أكثر
الكاتيونات ♣
يرمز لها برمز الذرة التي فقدت الإلكترونات مع إضافة إشارات + تدل على عدد الإلكترونات المفقودة يمين أعلى الرمز
♣الأنيونات
يرمز لها برمز الذرة التي اكتسبت الإلكترونات مع إضافة عدد من إشارات -يمين أعلى الرمز تدل على عدد الإلكترونات المكتسبة
جدول توضيحي شحنته الكهربائية العدد الذري نوعه صيغته إسم الأيون +2e Z=29 كاتيون Cu2+ ايون النحاس اا +3e Z=26 كاتيون Fe3+ ايون الحديد ااا -1e Z=17 أنيون Cl- أيون الكلورور +3e Z=13 كاتيون Al3+ أيون الألومنيوم ااا -2e Z=8 أنيون O2- ايون الاوكسجين
الأيونات المتعددة الذرات
♣جدول توضيحي 
شحنة الأيون نوع الأيون رمز الأيون إسم الأيون -1e OH- أيون الهيدروكسيد -2e SO42- أيون الكبريتات -1e NO3- أيون النترات +1e NH4+ أيون الأمونيوم استنتاج
الأيونات المتعددة الذرات هي مجموعة من الذرات اكتسبت أو فقدت إلكترون أو أكثر
 13 commentaires
13 commentaires Suivre le flux RSS des articles de cette rubrique
Suivre le flux RSS des articles de cette rubrique Suivre le flux RSS des commentaires de cette rubrique
Suivre le flux RSS des commentaires de cette rubrique
بسم الله الرحمان الرحيم